Virusurile produc infecții precum gripa, COVID-19 sau SIDA. Cercetările au arătat însă ca acestea au jucat și un rol cheie în evoluția speciei umane.
Oamenii au devenit familiari cu infecțiile precum Zika, Ebola, gripa, chiar și cu răceala comună. Dar, deși este cunoscut faptul că acestea îmbolnăvesc oamenii, surprinzător, de-a lungul a milioane de ani, corpul uman s-a adaptat la ele.
Cum acționează virusurile?
Virusurile reprezintă mai mult decât un șir de gene,de obicei sub forma unei molecule numite ARN, acoperite de un strat proteic, toate operând în același mod de bază.
Odată ce un virus a infectat o celulă, acesta modifică propriul mecanism molecular al acesteia, cu scopul de a produce propriile gene și proteine virale. În urma acestui proces, se creează noi molecule, care, în cele din urmă, izbucnesc în căutarea de noi celule pentru a le ataca.
Pentru majoritatea virusurilor, cum ar fi gripa, povestea se încheie aici. Însă, anumite retrovirusuri, inclusiv virusul HIV, se comportă mai ciudat, atacând ADN-ul. Acestea se inserează la întâmplare în genomul unui organism, până când apare momentul oportun pentru divizare și răspândire.
Odată ce un retrovirus a intrat în ADN-ul unui organism, nu există nicio garanție că acesta nu va migra. Instrucțiunile genetice pot fi „citite” din virusul încorporat, transformate în ADN,iar, ulterior, lipite într-o altă locație din genom. Repetarea acestui ciclu duce la multiplicarea rapidă a ADN-ului viral.
Pe parcursul a milioane de ani, în aceste secvențe ADN virale apar mutațiiși schimbări aleatorii, acesta pierzându-și capacitatea de a se elibera de celulele gazdă. Prinse în interiorul genomului, unele dintre aceste retrovirusuri „endogene” pot să își schimbe poziția în timp ce altelesunt blocate, pentru totdeauna, acolo unde s-au fixat.
În cazul în care,oricare dintre aceste evenimente are loc în celulele germinale care formează ovule și spermatozoizi, atunci acestea vor fi transmise de la o generație la alta și, în cele din urmă, vor deveni o parte permanentă a genomului.
Aproximativ jumătate din genomul uman este alcătuit din milioane de secvențe de ADN, care provin de la virusuri inactive de multă vreme sau de la alte gene similare, cunoscute colectiv ca elemente transpozabile sau transpozoni.
Unii cercetători sunt de părere că aceast procent ar putea fi chiar de 80%, deoarece secvențele antic edin genom sunt acum degradate dincolo de punctul de recunoaștere, asemenea unor fosilele moleculare.
Timp de mai mulți ani, segmente mari de ADN derivate din virus, care alcătuiesc genomul uman, au fost clasificate ca fiind „gunoi”. O proporție dintre aceste segmente repetitive este, fără îndoială, mai mult decât gunoi în codul nostru genetic, dar, pe măsură ce oamenii de știință privesc mai îndeaproape elementele virale individuale, apare o imagine mai sofisticată.
Evoluția sincitinei
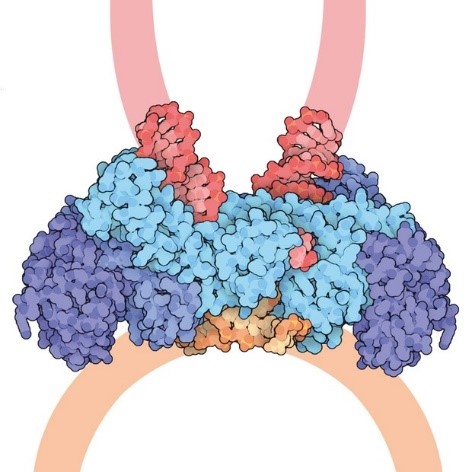
În urmă cu aproximativ 15 ani, cercetătorii americani au descoperit o genă umană care era activă doar în placentă. Ei au numit-o sincitină sau enverină, deoarece produce o moleculă care fuzionează celulele placentare împreună, creând un strat tisular cunoscut sub numele de sincitium. Totuși, este interesant faptul că sincitina seamănă foarte mult cu o genă provenită dintr-un retrovirus.
Ulterior, a fost descoperită o altă genă de sincitină, care este implicată și în formarea placentei, precum și pentru a preveni sistemul imunitar al mamei să atace fătul, în pântec. Din nou, gena a părut că ar provenii de la un retrovirus.
Cu toate acestea, în timp ce oamenii și alte primate de dimensiuni mari au aceleași două gene de sincitină, acestea nu se găsesc la niciun alt mamifer cu straturi celulare fuzionate în placentă.
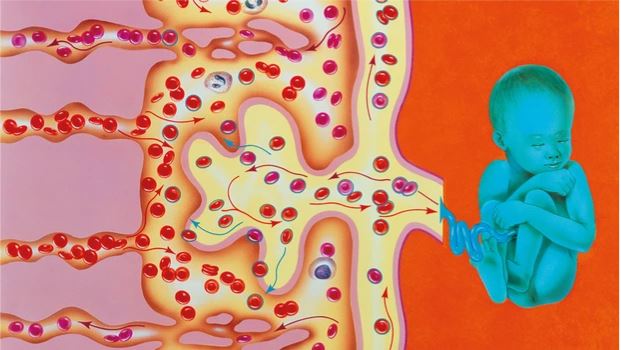
Șoarecii au, de asemenea, două gene de sincitină: au același mecanism ca cele umane, dar arată ca niște virusuri complet diferite. Există însă și o altă genă separată, derivată de la sincitină la pisici și câini, ambele descendente din aceiași strămoși carnivori.
În mod clar, toate aceste specii de mamifere au fost infectate de anumite virusuri, cu milioane de ani în urmă. De-a lungul timpului, aceste virusuri au fost valorificate pentru a juca un rol esențial în creșterea placentară, făcându-le să fie un dispozitiv permanent în genomul nostru.
În mod intrigant, porcii și caii nu au un strat de celule care fuzionează în placentă și, de asemenea, nu au gene care să semene cu sincitinele virale derivate. Așadar, este probabil ca aceste specii să nu ficontractatniciodată unul dintre aceste virusuri care fuzionează.
Genele transpozabile
În timp ce cazul sincitinei dezvăluie adoptarea unei gene de virus în genomul uman, există multe alte exemple cu privire la modul în care secvențele virale antice pot influența activitatea genelor oamenilor în prezent.
În anii ’50, o lucrare amănunțită și detaliată a geneticianului american Barbara McClintocka dezvăluit faptul că „genele săritoare” ar putea afecta genomul porumbului.
La fel ca „genele săritoare”, identificate de către McClintock la porumb, retrovirusurile endogene, care se ascund în genomul uman, au fost în mișcare de-a lungul a milioane de ani, schimbându-și poziția în mod aleatoriu și modificând activitatea genelor din imediata lor vecinătate.

Celulele umanefolosesc multă energie în încercarea de a opri deplasarea acestor elemente virale. Acesteasunt etichetate și blocate cu etichete chimice, cunoscute sub numele de mărci epigenetice. Cu toate acestea, pe măsură ce elementele virale se mișcă, aceste etichete moleculare se deplaseazăîmpreuna cu ele, astfel încât efectele secvențelor virale se pot răspândi la genele vecine.
În schimb, secvențe de ADN ale virusurilor atrag molecule care activează genele. Într-un retrovirus activ, aceste „comutatoare” activează genele virale în așa fel încât acestea pot deveni din nou infecțioase. Totuși, atunci când o secvență asemănătoare virusului se mută într-o altă regiune din genom, această abilitate de a acționa ca un comutator genetic poate ajunge să fie nocivă.
În anul 2016, oamenii de știință de la Universitatea din Utah, au descoperit faptul că un retrovirus endogen din genomul uman, care provenea inițial de la un virus care i-a infectat pe strămoșii noștri în urmă cu aproximativ 45-60 de milioane de ani, activează o genă numită AIM2, atunci când detectează o moleculă numită Interferon. Această moleculă reprezintă „semnalul de pericol”, care avertizează organismul că suferă o infecție virală. AIM2 obligă apoi celulele infectate să se autodistrugă, pentru a preveni răspândirea infecției.
Aceste virusuri antice au devenit „agenți dubli”, ajutând celulele umane să facă față altor virusuri care încearcă să le atace.
Un alt exemplu de virus care a avut un rol în evoluția speciei umane, se găsește în vecinătatea unei gene numite PRODH. Aceasta se găsește în celulele creierului, în special în hipocamp.
În cazul oamenilor, gena este activată cu ajutorul unui comutator ce are la bază un retrovirus inactiv. Cimpanzeii prezintă, de asemenea, o versiune a genei PRODH, dar nu este atât de activă ca în cazul oamenilor.
O posibilă explicație a apariției acestuia este că un virus antic și-a translatat o copie a sa în vecinătatea genei PRODH, cu milioane de ani în urmă, dar că acest lucru nu s-a întâmplat în cazul primatelor ancestrale, care au continuat să evolueze, devenind cimpanzeii de astăzi.
În zilele de astăzi, se consideră faptul că anumite tulburări ale creierului au la bază o funcționalitate incorectă a PRODH.
În mod similar, variațiile întreruptoarelor genetice sunt responsabile de diferențele dintre celulele care alcătuiesc fețele umane pe măsură ce creștem în pântec. La fel se întâmplă și în cazul cimpanzeilor. Deși genele umane sunt practic identice cu genele cimpanzeului, oamenii nu arată la fel ca aceste primate. Așadar, diferența este dată de întrerupătoarele de control.
Judecând după secvențele lor de ADN, multe dintre comutatoarele care sunt active în celulele care alcătuiesc fețele umane par să provină inițial de la virusuri care au avut rol în evoluția speciei.
Controlul virusurilor
Pe lângă căutarea de virusuri antici inactivi care au modificat biologia umană, oamenii de știință mai investighează și mecanisme de control care stau la baza efectelor acestora. Vinovații cheie sunt niște molecule speciale, numite KRAB Zinc Protein Finger (KRAB ZFPs), care captează secvențele virale din genom și le fixează.
Profesorul Didier Trono, împreună cu echipa sa, de la Universitatea din Lausanne, Elveția, a descoperit peste 300 de ZFP-uri KRAB diferite în genomul uman, fiecare dintre ele preferând o porțiune diferită de ADN derivat viral. Odată ajunși în zona țintită, ele ajută stimularea mecanismelor care activează sau dezactivează genele.
„Aceste ZFP KRAB au fost considerate„ucigași” ai acestor retrovirusuri endogene, explică Trono. „Cu toate acestea, ajută la exploatarea la maxim a secvențelor virale.”
Trono și echipa sa susțin faptulcă ZFP KRAB reprezintălegătura lipsă dintre secvențele virale care sunt activ dăunătoare și cele care au devenit comutatoare de control.
Ei au dovezi care atestă faptul că proteinele au evoluat alături de elementele virale într-un fel de „cursă de înarmare”, inițial suprimându-le, iar în cele din urmă, copleșindu-le.
„Noi credem că ceea ce facZFP KRAB este să țină sub control aceste elemente”, declară Trono. „Prin ținere sub control, mă refer nu doar la asigurarea faptului că virusurile nu mai translatează, ci la faptul că îi transformă în ceva benefic pentru gazdă, care reprezintă un mod foarte rafinat de reglare a activității genice în toate celulele și situațiile posibile.”
Susținerea acestei idei este constatarea faptului că, grupuri distincte de KRAB ZFP sunt active în diferite tipuri de celule. De asemenea, se găsesc în modele specifice ale diferitelor specii.
Dacă rolul lor era doar acela de a suprima virusurile, ar fi trebuit să fie prezente în toate celulele, aceeași serie de proteine. Ba mai mult, de ce de aceste proteine sunt legate miile de elemente virale inactive de multă vreme, pe care Trono și echipa sa le-au identificat?
Nu are niciun rost suprimarea unui retrovirus inactiv, așa că, acestea trebuie să joace un rol important în controlul activității genice.
Deși ideea lui este încă puțin controversată, Trono vede ZFP KRAB ca pe niște elemente de control ale virusurilor, transformându-le în comutatoare genetice.
De-a lungul a milioane de ani, acestea ar fi putut fi un motor puternic pentru crearea de noi specii. De exemplu, dacă un virus este transmis la întâmplare la o anumită creatură ancestrală și nu la alta, iar acesta este ulteriorcontrolată de ZFPKRAB, se creează noi comutatoare de control, care ar putea avea un impact mare asupra aspectului sau comportamentului unui animal.
Ba mai mult, aceste elemente devin mai active în urma schimbărilor de mediu. Pe măsură ce vremurile se schimbă, speciile trebuie să găsească noi modalități de adaptare pentru a supraviețui.
Activarea acestor elemente mobile modifică genomul, acest lucru aducând noi variații genetice care asigură evoluția speciei.
Virusuri: avantaje, dezavantaje și beneficii
Este clar că virusurile prinse în genomul uman au adus beneficii enorme de-a lungul evoluției. Cu toate acestea, nu sunt chiar atât de utile. Aproximativ 1 din 20 de copii se naște cu un nou „salt” viral, undeva în genomul său, fapt care ar putea dezactiva o genă importantă și care ar putea provoca o boală.
Există dovezi din ce în ce mai mari, potrivit cărora modificările transpozonilor contribuie la haosul genetic din celulele canceroase. Cercetările sugerează faptul că celulele creierului sunt locațiile cele mai facile pentru reactivarea genelor „săritoare” care pot duce la creșterea diversității celulelor nervoase și îmbunătățirea puterii cerebrale.Totuși, acestea pot provoca probleme de memorie și condiții legate de îmbătrânire, cum ar fi schizofrenia.
Așadar, virușii din ADN-ul uman sunt buni sau răi? Paolo Mita, un postdoctorand care cercetează transpoziții în cadrul Școlii de Medicină din New York, sugerează faptul că acest lucru reprezintă câte un pic din ambele.
„Pe termen scurt, ei sunt dușmanii noștri. Pe de altă parte, dacă ne uităm de-a lungul timpului, acestea reprezintă un element puternic al evoluției, fiind încă active în specia noastră chiar și în prezent”.
„Evoluția constă doar modul în care organismele răspund la schimbările din mediu și, fiind în acest caz, prietenii noștri, deoarece au format modul în care genomul nostru funcționează acum.”
Totuși,virusurile care ne infectează astăzi, cum ar fi HIV, vor avea un impact asupra evoluției noastre în viitor?
„Desigur! Răspunsul este de ce nu”, a declarat Mita. „Dar vor trece multe generații până când vom putea privi înapoi și vom spune că această evoluție s-a întâmplat. Putem vedea în genom rămășițele bătăliilor anterioare dintre retrovirusurile endogene și celulele gazdă. Este o luptă continuă și nu cred că s-a oprit vreodată.”