Cercetătorii au modificat genetic un tip de bacterii, în așa fel încât acestea să pătrundă în interiorul celulelor imunitare ale șoarecilor, pentru a elibera proteine care schimbă comportamentul acelor celule. Lucrarea este un prim pas către crearea „endosimbioților artificiali” care ar putea trăi în interiorul unor celule ale corpului uman și ar putea efectua tot felul de procese, de la ghidarea regenerării țesuturilor deteriorate și până la tratarea cancerului.
„Aceasta este viziunea pe termen lung”, a declarat Christopher Contag din cadrul Universității de Stat din Michigan.
De asemenea, în prezent, alte câteva grupuri de cercetători dezvoltă diferiți endosimbioți artificiali, despre care se spune că ar putea permite optimizarea creșterii culturilor și animalelor de fermă și tratarea afecțiunilor legate de înaintarea în vârstă.
„Inițial, ideea de a crea endosimbioți artificiali era considerată drept fiind fantezistă. Totuși, datorită progreselor uriașe din ultimii ani, în ceea ce privește dezvoltarea organismelor, aceasta începe să fie văzută ca fiind fezabilă. Acesta va fi una dintre cele mai mari inovații din viitorul foarte apropiat. În ultimii cinci ani, am observat un interes enorm în acest domeniu”, a declarat Bogumil Karas din cadrul Universității Ontario de Vest din Canada,
Majoritatea organismelor depind de microbii care trăiesc pe sau în ele (microbiom). Totuși, uneori, relația este și mai apropiată. Unele bacterii trăiesc în interiorul celulelor plantelor sau animalelor într-o relație avantajoasă pentru ambele părți, denumită endosimbioză.
Endosimbioții pot oferi organismelor abilități vitale pentru supraviețuirea lor. Structurile producătoare de energie din toate celulele animale și vegetale au evoluat din bacterii endosimbiotice. Același lucru se poate spune și despre structurile fotosintetice din toate celulele vegetale.
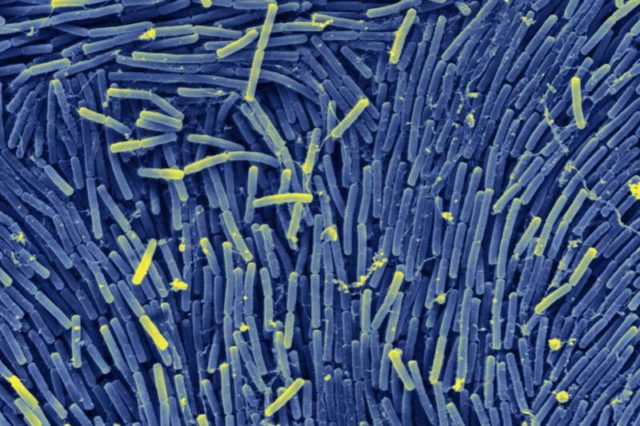
Pentru a crea un endosimbiont de la zero, echipa lui Contag a utilizat o bacterie denumită Bacillus subtilis, care se regăsește la nivelul intestinului oamenilor. „Este o bacterie normală, care face parte din microbiomul uman”, a declarat Cody Madsen, membru al echipei în cadrul Universității de Stat din Michigan.
Cercetătorii au proiectat endosimbiontul în așa fel încât acesta să producă proteine care modifică activitatea genelor. Astfel, comportamentul celulelor mamiferelor poate fi controlat.
Pentru a introduce bacteriile în celulele de șoarece, Contag, Madsen și colegii lor s-au bazat pe faptul că unele celule animale pot absorbi bacteriile printr-un proces numit fagocitoză. În mod normal, bacteriile absorbite rămân prinse în saci de membrană, unde sunt digerate. Totuși, tulpina modificată de B. subtilis secretă o proteină care îi permite să iasă din acești saci.
Cercetătorii au implantat bacteriile modificate într-o cultură de celule imunitare de șoarece, cunoscute sub numele de macrofage, care au fost crescute într-un vas. Ei au reușit să introducă bacteriile în 99% dintre celule. De asemenea, cercetătorii au arătat faptul că proteinele, pe care bacteriile au fost concepute pentru să le producă, au modificat comportamentul macrofagelor.
În prezent, cercetătorii încearcă facă bacteriile să trăiască în armonie cu noile lor gazde. La două zile după implantare , 10% dintre macrofage au fost ucise de bacteriile din interiorul lor, care s-au divizat și s-au reprodus prea rapid.
„Următorul pas este adăugarea unui circuit genetic, care va controla înmulțirea bacteriilor în așa fel încât acestea să se dividă doar atunci când celula gazdă se divide”, a declarat Madsen,
De asemenea, echipa intenționează să modifice bacteriile în așa fel încât acestea să poată fi controlate odată ce se află în interiorul unui organism (prin substanțe chimice sau câmpuri magnetice, avantajul utilizării magnetismului fiind obținerea unui control localizat).
„Celulele în care există acești endosimbioți ar putea fi transformate în celule stem și apoi într-un alt tip de celulă”, a explicat Contag.
„Astfel de comutatoare ar putea fi folosite și pentru a ucide bacteriile dacă este necesar”, a adăugat Madsen.
„Faptul că echipa de cercetare a reușit să introducă bacteriile într-o populație atât de mare de celule este incredibil. Totuși, realizarea acestui lucru într-un organism viu și în alte tipuri de celule va fi mult mai dificilă. Supraviețuirea acestora pe termen lung este, în mod evident, crucială”, a declarat Karas.